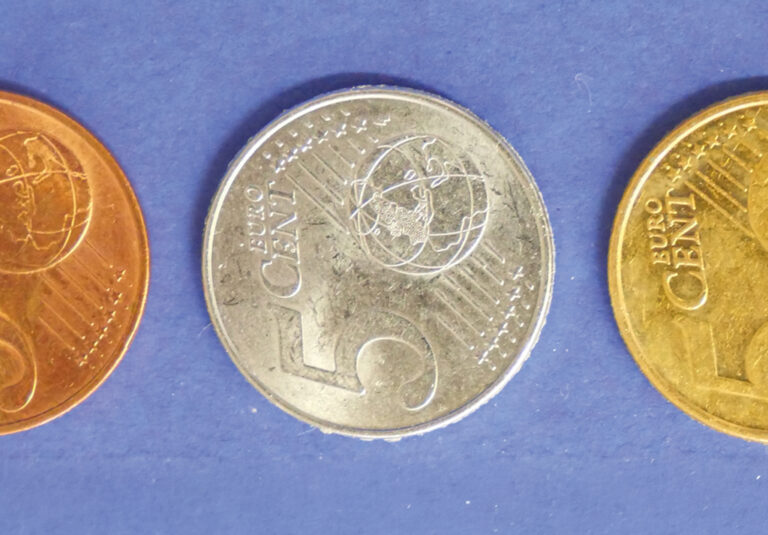Brandgefährliche Chemie-Experimente
Es ist ein beliebter Versuch im Chemieunterricht an Schulen: „Vergolden einer Kupfermünze“. Doch im Nachgang des Experimentes kommt es immer wieder zu Brandschäden, die sich zumeist als Mülleimerbrände darstellen. Was läuft schief? Was muss getan werden, um derartige Schäden zu verhindern?
„Hier hat Lehrer Krawumm Chemie unterrichtet“ – unter dieser Schlagzeile berichtet die Bild-Zeitung bereits im Jahr 2015 über einen Brandschaden im Chemieraum eines Hamburger Gymnasiums.[1] Der Lehrer habe den Schülern einer 8. Klasse das Experiment „Vergolden einer Kupfermünze“ vorgeführt. Mit Zinkpulver, Natronlauge und einem Bunsenbrenner habe er ein Centstück golden verfärbt. Das zurückbleibende Pulver sei von dem Lehrer mit Wasser abgespült und in einem Mülleimer entsorgt worden. Nach rund zwei Stunden hätten sich die Versuchsreste in dem Mülleimer entzündet und einen Schaden von 67.000 Euro verursacht. Doch der Strafprozess gegen den Lehrer endete mit einem Freispruch: Es sei nicht zu ermitteln gewesen, was genau den Brand in dem Mülleimer verursacht habe.
Schadenhäufung
Das beschriebene Schadenereignis ist kein Einzelfall. Das IFS hat bundesweit bereits zahlreiche Fälle untersucht, in denen es nach dem Schulversuch „Vergolden einer Kupfermünze“ zu Bränden gekommen ist (Schadenfälle A bis E). Ein brandursächlicher technischer Defekt war stets auszuschließen. Auch eine Brandverursachung durch unbekannte Dritte kam nicht in Betracht, da die brandbetroffenen Chemieräume außerhalb der Unterrichtszeit verschlossen waren. Der Brandherd in den Chemieräumen war stets auf den Abstellort des Müllereimers einzugrenzen. Die Schadenhäufung lässt vermuten, dass ein methodischer Fehler vorliegt, der zu den Bränden führte.
SCHADENFALL A | Am Samstag fand bis ca. 17:00 Uhr an der Schule ein Tag der offenen Tür statt. Im Chemietrakt war unter anderem der Versuch „Vergolden einer Kupfermünze“ vorgeführt worden. Bemerkt wurde der Brand am Montagmorgen gegen 06:00 Uhr. Der Brand am Standort des Kunststoffmülleimers (Pfeil) war bereits von selbst erloschen.

SCHADENFALL B | In der 3. Unterrichtsstunde wurde das Experiment „Vergolden einer Kupfermünze“ durchgeführt. Die Überreste wurden in einem Kunststoffmülleimer neben der Tafel entsorgt. In der nachfolgenden Unterrichtsstunde war der Chemieraum unbelegt und verschlossen. Der Brand im Bereich des Mülleimers (Pfeil) wurde dann zu Beginn der 5. Unterrichtsstunde bemerkt.

SCHADENFALL C | Auch hier wurde im Chemieunterricht das Experiment „Vergolden einer Kupfermünze“ durchgeführt. Durch die automatische Brandmeldeanlage wurde der Brand im Aufstellbereich des Mülleimers (Pfeil) bereits in der anschließenden großen Pause detektiert.

SCHADENFALL D | Es wurde im naturwissenschaftlichen Unterrichtsraum ein bereits selbsttätig erloschener Brandherd an dem Abstellort des Kunststoffmülleimers (Pfeil) bemerkt. In dem Raum war in der letzten Chemiestunde am Vortag der Versuch „Vergolden einer Kupfermünze“ durchgeführt worden.


SCHADENFALL E | Auch hier wurde der Versuch „Vergolden einer Kupfermünze“ durchgeführt. Die im Mülleimer des Chemieraumesentsorgten Versuchsüberreste waren von den Putzkräften bereits in den Müllsack ihres Putzmittelwagensüberführt worden, welcher aufdem Flur in Brand geriet (Pfeil). Die Überrestedes Putzwagens waren im Zuge der Löschmaßnahmenbereits ins Freie verbracht worden.

Messing – eine goldfarbene Legierung aus Kupfer und Zink
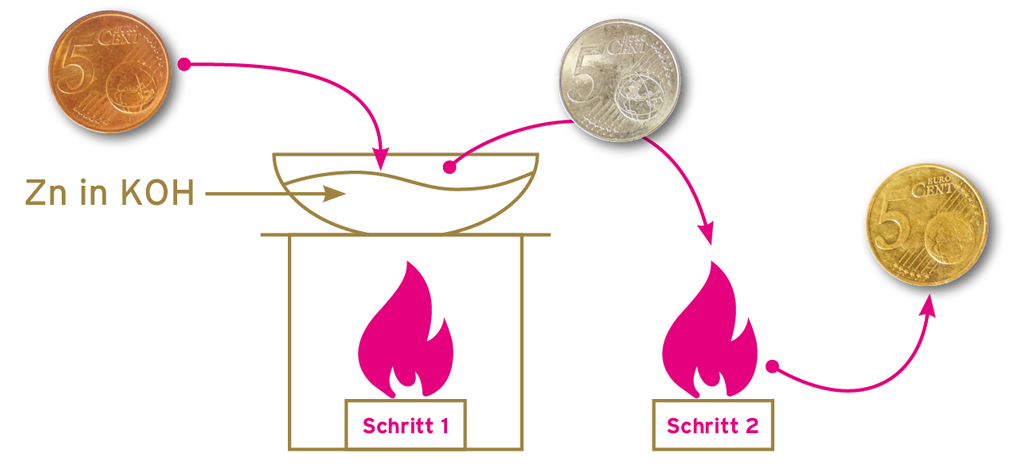
Auch wenn die Bezeichnung „Vergoldeneiner Kupfermünze“ anderes vermuten lässt, kommt Gold in dem gesamten Versuchsablauf nicht vor. Thema des Experimentes ist viel mehr Messing –eine Legierung aus Kupfer und Zink. Als Ergebnis des Versuchs lässt eineäußerliche Messingschicht die Kupfermünze lediglich goldfarben erscheinen (Grafik 1). Konkret läuft das Experiment „Vergolden einer Kupfermünze“ in zwei Schritten ab: In einem ersten Schritt wird die Kupfermünze mit alkalischem Zinkpulver erhitzt. Das Zinkpulver schlägt sich auf der Münze nieder und lässt diese zunächst silberfarben erscheinen. Wird diese Münze im zweiten Schritt in einer Brennerflamme erhitzt, bildet sich aus dem Kupfer der Münze und dem Zinküberzug an der Oberfläche eine goldfarbene Messingschicht (Bild 6).
Gefahrstoff Zinkpulver
Bei dem Experiment ist das Zinkpulverals selbstentzündlicher Gefahrstoff zu benennen. Zink ist ein unedles Metall. Es überzieht sich bereits an der Luft mit einer passivierenden Oxidschicht, die das Metall gräulich erscheinen lässt.
Weil das Zink in Pulverform eine große reaktive Oberfläche hat, läuft diese Oxidation im Kontakt mit Luftsauerstoff besonders schnell ab. Oft findet beim Experimentieren sogenanntes stabilisiertes Zinkpulver Verwendung. Zur Stabilisierung wird dem Zinkpulver bereits beim Herstellungsprozess gezielt Sauerstoff zugesetzt. So bildet sich um jedes Zinkstaubkorn eine dünne Schichtaus Zinkoxid. Dies sorgt dafür, dass die Reaktivität des Zinkstaubs reduziert ist. So wird die ungewollte chemische Reaktion zu Carbonaten und Oxiden vermindert und es werden „ungefährlichere“ Explosionskennwerte erzielt. [2]
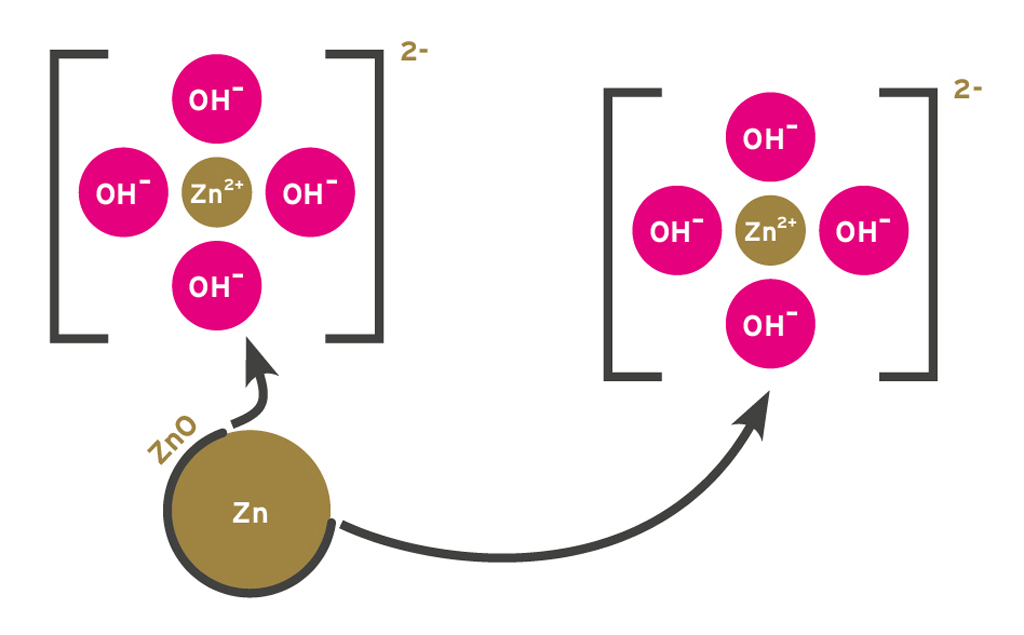
Um bei dem Experiment „Vergoldeneiner Kupfermünze“ die Durchmischung von Zink und Kupfer zu der Legierungzu erzielen, ist es notwendig, die passivierende Oxidschicht an dem Zinkpulver zu entfernen. Das geschieht im ersten Schritt des Versuchs in einer alkalischen Lösung (Grafik 2).
Was für die Versuchsdurchführung notwendig ist, wird jedoch bei der anschließenden Abfallentsorgung zum Problem. Kommt das durch die alkalische Behandlungvon der passivierenden Oxidschicht befreite Zinkpulver wieder in Kontaktmit dem Luftsauerstoff, bildet sich die Oxidschicht erneut aus. Das ist ein exothermer (= wärmeerzeugender) Vorgang. Kann die entstehende Wärme z. B. innerhalb eines Mülleimers nicht abgeführt werden, beschleunigt sich die Reaktion selbst. Binnen kurzer Zeit kann die Selbsterwärmung so in eine Selbstentzündung übergehen. Die Brände sind also auf eine unsachgemäße Entsorgung der sehr reaktiven alkalischen Zinkpulverreste zurückzuführen.
REALE BRANDVERSUCHE
Das Landeskriminalamt Baden-Württemberg hat im Rahmen der Ursachenforschung zu einem Brandschaden eigene Brandversuche durchgeführt. Diese Versuche führen die von dem alkalischenZinkpulver ausgehende Gefahr der Selbstentzündung deutlich vor Augen:








Bilder 7 bis 9 / Das mit einem Faltenfilter abfiltrierte alkalische Zinkpulverwird zur Erzeugung eines Wärmestaus abgedeckt und entzündet sich daraufhin selbst.
Bilder 10 bis 14 / Die in einem Kunststoffmülleimer entsorgten Überrest eaus dem Versuch „Vergolden einer Kupfermünze“ entzünden sich selbst und führen zum Brand des Mülleimers.
Prüfung des Selbstentzündungspotenzials
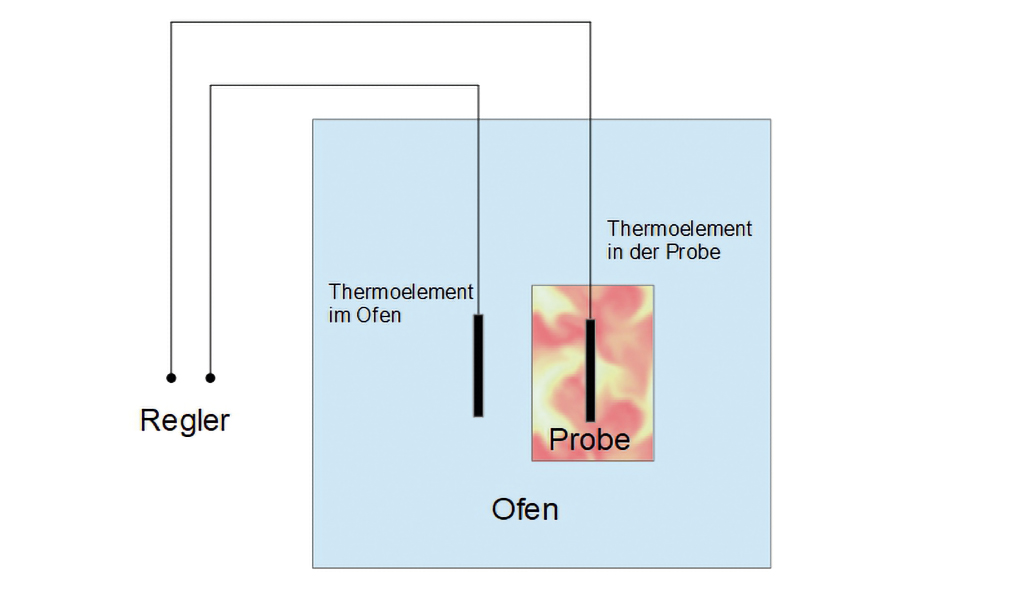
Das Selbstentzündungsverhalten verschiedener Stoffe wird im Labor des IFS standardmäßig in einer speziellen Messapparatur untersucht.[3] Die Apparatur besteht aus einem elektrisch beheizbaren Ofen, der durch ein vorzugebendes Temperaturprogramm computergesteuert hochgeheizt wird. Die zu untersuchende Probe befindet sich in dem Ofen. Die Probe ist ebenso wie der Ofen mit einem Temperaturfühler versehen, der die Temperaturentwicklung beim kontrollierten Hochheizen des Ofens aufzeichnet (Grafik 3).
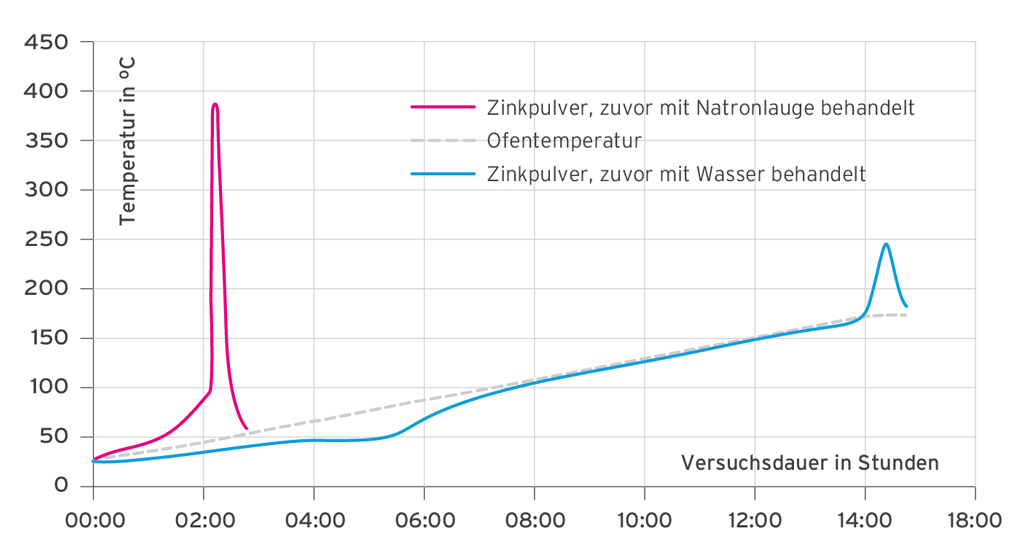
Mit der Apparatur wurden unter identischen Bedingungen nacheinander zwei Proben untersucht – zum einen ein zuvor mit Natronlauge erhitztes Zinkpulver und zum anderen ein Zinkpulver, das in gleicher Weise lediglich mit Wasser behandelt wurde. Der direkte Vergleich der beiden aufgezeichneten Kurven zeigt, dass bei dem mit Natronlauge behandelten Zinkpulver bereits nach zwei Stunden ein Temperaturanstieg von annähernd 400 °C zu messen ist, während bei dem lediglich mit Wasser behandelten Zinkpulver ein deutlich schwächerer Temperaturanstieg nach erst 14 Stunden eintritt (Grafik 4).
FAZIT
Zur Schadenverhütung ergeben sich folgende Ansatzpunkte:
- Die selbstentzündlichen Zinkpulverreste waren in einfachen Mülleimern aus Kunststoff entsorgt worden. Die Verwendung von selbstlöschenden und feuerfesten Abfallbehältern (Bilder 15 und 16) hätte in den Schadenfällen A bis D sicher bereits viel Schaden verhindert.
- Letztlich schadenursächlich ist die unsachgemäße Entsorgung der Versuchsreste. Die aus dem Experiment stammenden Zinkpulverreste dürfen nicht in den Mülleimer gegeben werden. Sie sind in den Behältern für Schwermetalle zu sammeln und dann über einen Entsorgungsbetrieb fachgerecht zu beseitigen.
- Bei der zu erstellenden Gefährdungsbeurteilung zu dem Experiment ist die von den Zinkpulverresten ausgehende Selbstentzündungsgefahr zu berücksichtigen.
- Von den verantwortlichen Chemielehrkräften wird die Selbstentzündungsgefahr zum Teil offenbar unterschätzt. Hier bedarf es weiterer Aufklärung.

Danksagungen: an Chiara Stöcker, Pablo Zamora und Dr. Dana Wächter (alle IFS) für die Durchführung der Laborversuche; das Landeskriminalamt Baden-Württemberg für die freundliche Genehmigung zur Veröffentlichung der Bilder 7 bis 14.

LITERATUR | QUELLENANGABEN
[1] Bild-Zeitung vom 08.07.2015; am 28.03.2025 abgerufen unter https://www.bild.de/regional/hamburg/prozesse/hier-hat-ein-lehrer-krawumm-chemieunterrichtet 41694170.bild.html
[2] GESTIS-Stoffdatenbank zu „Zink, Pulver oder Staub, stabilisiert“; am 28.03.2025 abgerufen unter https://gestis.dguv.de/data?name=500052
[3] „Selbstentzündung – eine vermeidbare Schadenursache“, A. Moors, D. Wächter in schadenprisma 4/2024